Une patiente souffrant de méningiomes (tumeurs au cerveau) attribués au médicament Androcur a obtenu, lundi 2 juin, plus de 300 000 euros d’indemnisation des laboratoires Bayer, Viatris et Sandoz pour « défaut d’information » sur la molécule.
« Le tribunal déclare la SAS Bayer HealthCare, la SAS Sandoz, la SAS Viatris Santé (…) responsables des préjudices subis », ainsi que le médecin et le pharmacien de la patiente, écrivent les juges du tribunal civil de Poitiers. Selon Romain Sintès, avocat de la plaignante, ce jugement ouvre la porte à « une multiplication des procédures » d’indemnisation.
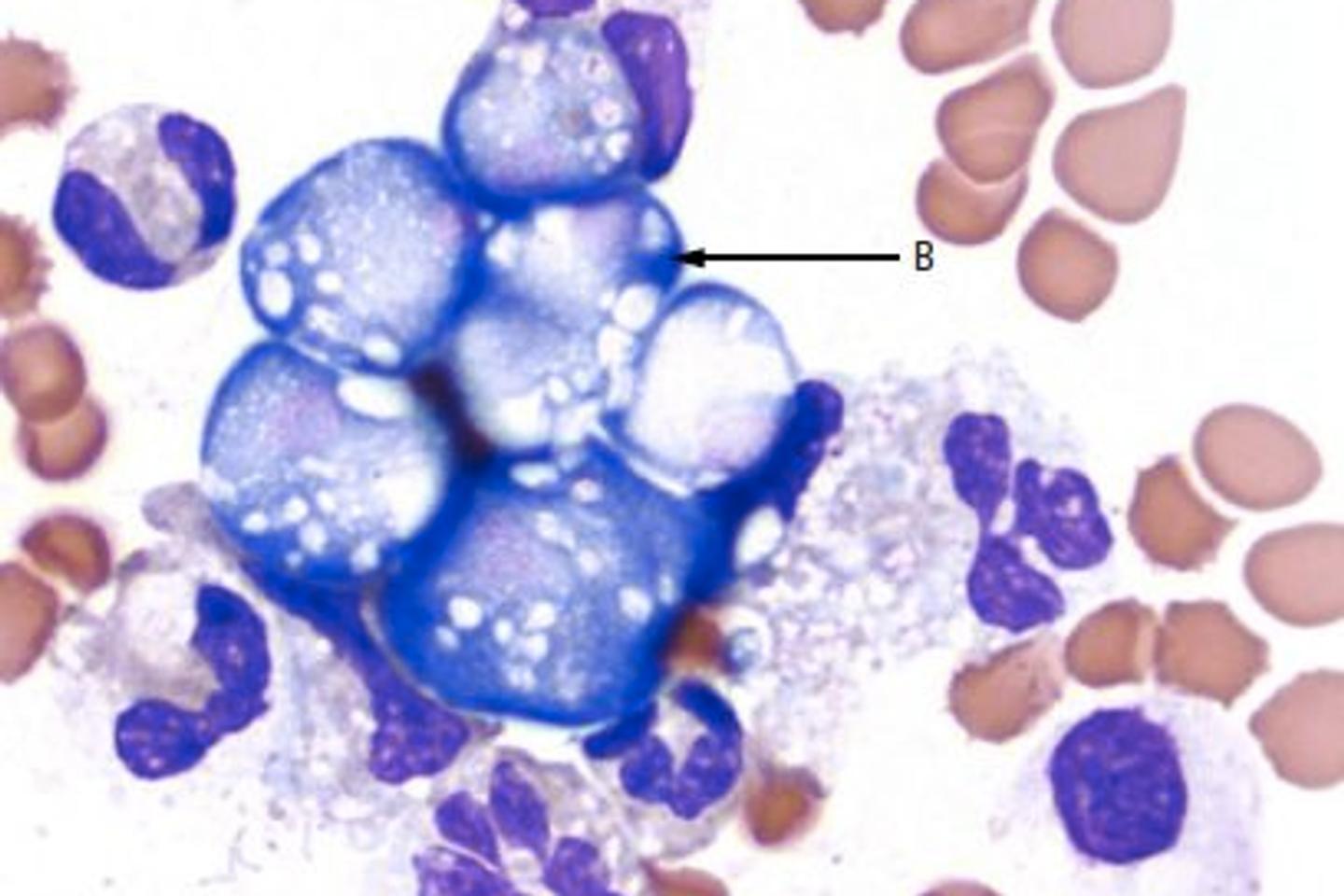
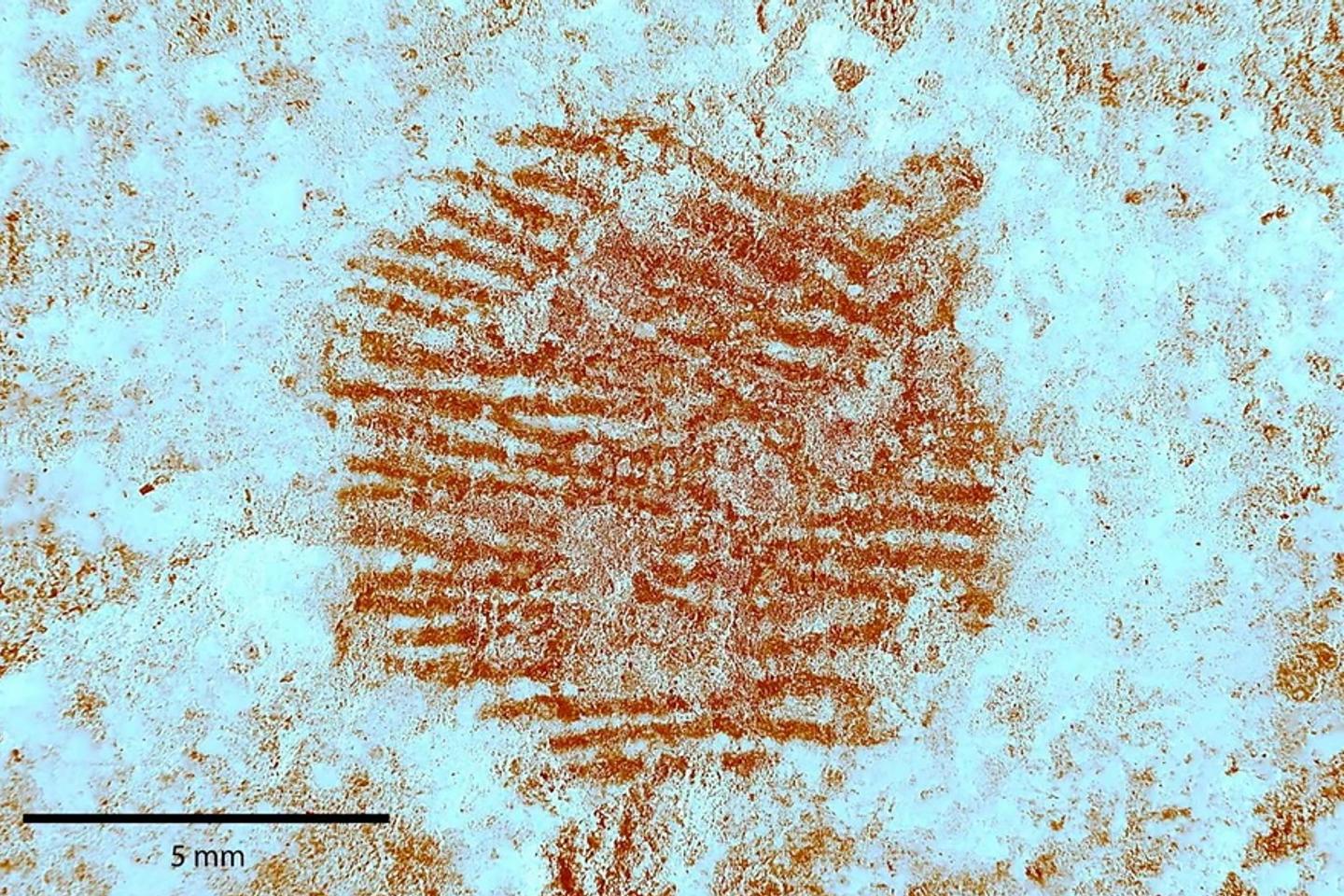
Cette femme âgée de 55 ans, qui a pris pendant plus de vingt ans ce traitement hormonal prescrit contre l’hyperpilosité ou encore l’endométriose, souffre depuis 2013 de multiples méningiomes, tumeurs non cancéreuses des membranes entourant le cerveau qui peuvent provoquer de graves handicaps neurologiques.
Souffrant aujourd’hui de troubles visuels, de la mémoire et de fatigue importante, la quinquagénaire assure ne pas avoir été prévenue des risques de l’Androcur, alors qu’un article scientifique évoquait dès 2008 un lien entre la molécule (acétate de cyprotérone) et l’apparition de méningiomes. Ce lien a été clairement établi en 2018 et le tribunal a jugé lundi que le dommage occasionné par la pathologie développée par la plaignante est bien « le résultat des traitements médicamenteux » qu’elle a suivis.
Effets graves et irréversibles
A l’audience en avril, Bayer avait allégué que la patiente n’avait pris l’Androcur que jusqu’en 2004, avant de suivre un traitement générique. « La SAS Bayer ne s’est pas donné tous les moyens pour assurer une information rapide et efficiente à destination finale des consommateurs, utilisateurs actifs ou anciens de l’Androcur, pour répondre aux exigences du devoir d’information », ont estimé les juges.
Selon Viatris, producteur d’une version générique, le risque n’était prouvé scientifiquement qu’à partir de 2019. Avant, la modification de la notice était de la responsabilité de l’Agence nationale de sécurité du médicament.
« La SAS Viatris Santé (ex-Mylan) ne s’est pas davantage donné les moyens, dès 2008 et a fortiori à compter de janvier 2011, pour permettre aux consommateurs (…) d’avoir connaissance du risque de méningiomes associés à [la] prise prolongée », fait valoir le tribunal, qui rend une conclusion similaire concernant Sandoz. Les laboratoires (à hauteur de 97 %), le médecin et le pharmacien sont condamnés à verser solidairement environ 325 000 euros, dont 25 % avec effet immédiat.
Pour M. Sintès, cette décision est à sa connaissance une première en France et constitue « la reconnaissance de ce défaut d’information de la communauté médicale ». « En dépit de ce que nous racontaient les laboratoires, ils avaient les moyens de communiquer sur des effets secondaires particulièrement graves, invalidants et surtout irréversibles, qu’ils connaissaient depuis 2008 », a-t-il dit à l’Agence France-Presse.